La aterosclerosis es ampliamente conocido al tratarse de una enfermedad inflamatoria crónica con posibles conexiones con infecciones cronificadas en el tiempo. Aunque los tratamientos antiinfecciosos no han demostrado ser efectivos en prevenir eventos cardiovasculares ateroscleróticos cada vez nos dotamos de un mayor conocimiento de su comprensión. A pesar de que incluso se ha comenzado a trabajar en en el desarrollo de una vacuna antiaterosclerótica, impulsadas por estudios en modelos animales que destacan la importancia de las respuestas inmunes innatas y adaptativas, deberíamos replantearnos varios escenarios, donde ese escenario principal sea comprender que el proceso de generación de placa puede ser sometido a un control cambiando nuestro estilo de vida y poniendo el foco en la inflamación.

Introducción
La aterosclerosis, conocida como una condición inflamatoria crónica, ha despertado un notable interés en la comunidad científica debido a sus posibles conexiones con infecciones crónicas. A lo largo de los años, diversos estudios epidemiológicos han sugerido que ciertos agentes infecciosos podrían estar vinculados con el desarrollo de enfermedades vasculares ateroscleróticas. A pesar de estas asociaciones, intentos por confirmar una relación causal directa, basándonos en los postulados de Koch, no han sido concluyentes. De hecho, numerosos ensayos clínicos han evaluado la efectividad de tratamientos antiinfecciosos en la reducción de eventos cardiovasculares relacionados con la aterosclerosis, pero los resultados han sido mayormente decepcionantes.
Los postulados de Koch son criterios desarrollados por el microbiólogo Robert Koch para demostrar que un microorganismo específico causa una enfermedad. Estos incluyen encontrar el patógeno en todos los casos de la enfermedad, aislarlo en cultivo puro, causar la enfermedad al introducirlo en un huésped sano, y reaislar el mismo patógeno del huésped experimentalmente infectado.
Este escenario ha llevado a los investigadores a profundizar en la comprensión de los mecanismos fisiopatológicos que podrían ser el origen de estas observaciones. Uno de los avances más prometedores en esta área ha sido el desarrollo de estrategias de vacunación dirigidas contra agentes infecciosos específicos, lo que ha abierto la puerta -nos guste o no, sea coherente o no- a la posibilidad de una vacuna antiaterosclerótica. Los estudios con modelos animales han sido fundamentales en este sentido, revelando que tanto las respuestas inmunes innatas como las adaptativas juegan roles críticos en el desarrollo de la aterosclerosis.
En este artículo vamos a explorar más a fondo la relación entre infecciones crónicas y aterosclerosis y revisaremos la evidencia procedente tanto de estudios en animales como en humanos. Esta perspectiva no solo nos ofrece un vistazo a la complejidad de la aterosclerosis como enfermedad inflamatoria, sino que también nos desafía a pensar en soluciones innovadoras que podrían transformar el enfoque preventivo en la salud cardiovascular.
¿Qué es la aterosclerosis?
La aterosclerosis es actualmente reconocida como una enfermedad inflamatoria crónica, un entendimiento que ha reformulado profundamente nuestra percepción sobre su naturaleza y tratamiento. En este contexto, las infecciones crónicas emergen como un factor crítico que puede desencadenar y perpetuar la inflamación sistémica que caracteriza a esta enfermedad. Se ha observado que ciertos microorganismos, tanto bacterias como virus, impactan directamente en el endotelio vascular. Además, tienen un efecto indirecto a través de la liberación de citocinas que, en conjunto, pueden acelerar el proceso aterosclerótico.
Entre los patógenos implicados se encuentran Chlamydia pneumoniae, Porphyromonas gingivalis, Helicobacter pylori, así como los virus de influenza A, hepatitis C, citomegalovirus (CMV) y el virus de la inmunodeficiencia humana (VIH). Cabe destacar, sin embargo, que la robustez de los datos que apoyan la relación entre cada uno de estos agentes y la aterosclerosis varía considerablemente.
La investigación reciente ha puesto de manifiesto la relevancia de la respuesta inmunitaria en la progresión de la aterosclerosis. Un descubrimiento particularmente intrigante es el mimetismo molecular entre el colesterol oxidado de las lipoproteínas de baja densidad (ox-LDL) y los polisacáridos de las paredes celulares bacterianas.
Mimetismo Molecular
El concepto de mimetismo molecular se origina mediante una situación donde las estructuras moleculares de diferentes orígenes biológicos se parecen lo suficiente como para confundir al sistema inmunitario. Este fenómeno puede tener implicaciones significativas en diversas enfermedades, incluida la aterosclerosis. La idea de que el colesterol oxidado de las lipoproteínas de baja densidad (ox-LDL) y los polisacáridos de las paredes celulares bacterianas muestran similitudes estructurales es especialmente importante en este contexto.

Mecanismos del Mimetismo Molecular en la Aterosclerosis
1. Iniciación de Respuestas Inmunitarias: Cuando el LDL en la sangre se oxida, las moléculas de ox-LDL resultantes cambian su estructura. Estas ox-LDL modificadas pueden asemejarse a los antígenos encontrados en las paredes celulares de ciertas bacterias. El sistema inmunitario, al detectar estas estructuras similares, puede iniciar una respuesta inmunitaria no solo contra la bacteria que imita, sino también contra el ox-LDL.
2. Formación de Placas de Ateroma: El reconocimiento inmunológico de ox-LDL debido a su similitud con los antígenos bacterianos puede llevar a una respuesta inflamatoria crónica. Los macrófagos, que son células del sistema inmunitario, engullen ox-LDL, transformándose en células espumosas que se acumulan en las paredes de las arterias. Esta acumulación contribuye a la formación de las placas de ateroma, las cuales son características de la aterosclerosis.
3. Aceleración del Proceso Aterosclerótico: Dado que el sistema inmunitario puede confundir ox-LDL con invasores bacterianos, la respuesta inflamatoria se mantiene y potencia, lo que acelera el proceso aterosclerótico. Esta reacción inmunitaria sostenida no solo promueve la formación de más placas, sino que también puede hacerlas más inestables y susceptibles a rupturas, lo que aumenta el riesgo de eventos cardiovasculares graves como ataques cardíacos o accidentes cerebrovasculares.
 Fases de la Aterogénesis y Efectos Patogénicos Asociados
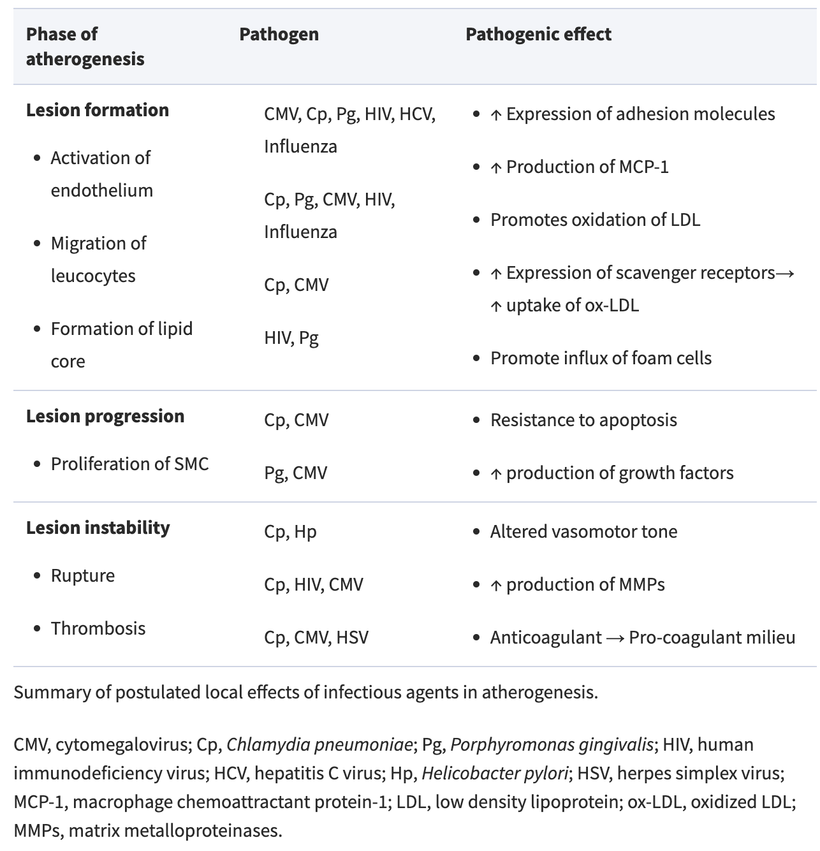
Fases de la Aterogénesis y Efectos Patogénicos Asociados
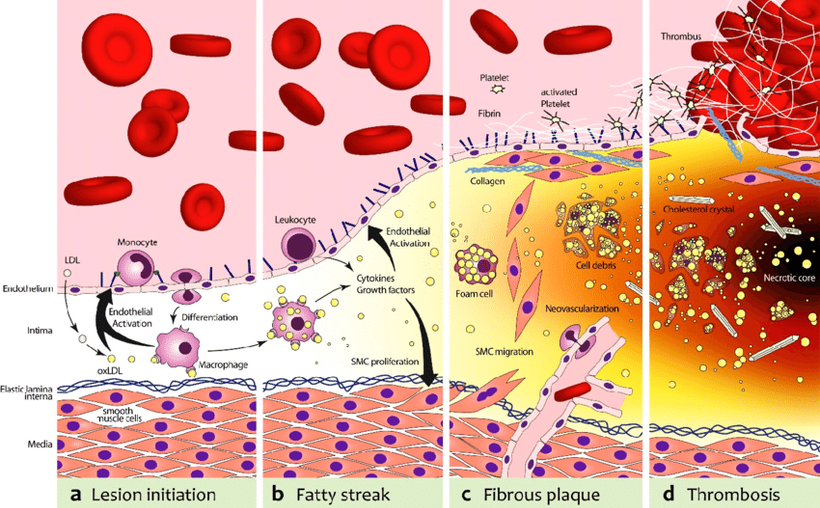
1. Formación de la lesión:
-
Activación del endotelio: Algunos microorganismos como el virus de la citomegalovirus, Chlamydia pneumoniae, Porphyromonas gingivalis, VIH, hepatitis C y el virus de la influenza pueden activar las células que recubren el interior de las arterias. Esto hace que estas células atraigan y retengan a los leucocitos (células blancas de la sangre), que se pegan a las paredes de las arterias.
-
Migración de leucocitos: Los mismos microorganismos también pueden producir señales químicas que atraen más células inflamatorias al lugar donde se está formando la lesión.
-
Formación del núcleo lipídico: Chlamydia pneumoniae y el virus de la citomegalovirus pueden hacer que el colesterol LDL se oxide, mientras que el VIH y Porphyromonas gingivalis aumentan la captura de este colesterol LDL oxidado, lo que lleva a la acumulación de células grasas y al desarrollo de lo que se llama el núcleo lipídico de la placa que obstruye las arterias.
2. Progresión de la lesión:
-
Proliferación de células musculares lisas: Chlamydia pneumoniae y el virus de la citomegalovirus pueden estimular la multiplicación de las células musculares en las paredes de las arterias, lo que contribuye a su engrosamiento.
-
Resistencia a la muerte celular y aumento de factores de crecimiento: Porphyromonas gingivalis y el virus de la citomegalovirus pueden hacer que las células sean más resistentes a morir y producir más factores que estimulan el crecimiento celular.
3. Inestabilidad de la lesión:
-
Ruptura y trombosis: Chlamydia pneumoniae y Helicobacter pylori pueden afectar la contracción y relajación de las arterias, mientras que Chlamydia pneumoniae, VIH y el virus de la citomegalovirus pueden producir enzimas que degradan las estructuras de las arterias, lo que puede llevar a su ruptura. Además, varios microorganismos pueden aumentar el riesgo de formación de coágulos sanguíneos.
¿La Solución? Más Bernard que Pasteur
Cuando hablamos de los fundamentos de la microbiología y la medicina moderna, las contribuciones de Robert Koch, Louis Pasteur y Claude Bernard son esenciales. Cada uno de estos científicos aportó teorías y métodos que no solo transformaron el entendimiento de las enfermedades, sino que también delinearon caminos para el desarrollo de la medicina.
Louis Pasteur: La Teoría Microbiana de la Enfermedad
Louis Pasteur es quizás más conocido por su desarrollo de la teoría microbiana de la enfermedad. Contrario a la creencia prevalente de la generación espontánea, Pasteur demostró que los microorganismos causan fermentación y enfermedades.
Robert Koch: Los Postulados de Koch
Formuló los postulados de Koch, que son criterios, que como describí arriba, deben cumplirse para establecer que un organismo es la causa de una enfermedad específica. Estos postulados establecen que el microorganismo debe estar presente en todos los individuos con la enfermedad y no en los sanos, debe ser aislado y cultivado en cultivo puro, y cuando se introduce en un nuevo huésped susceptible, debe causar la enfermedad original. A través de este método, Koch identificó los causantes de enfermedades como el cólera y la tuberculosis, revolucionando el campo de la bacteriología.
Claude Bernard: El Principio de la Homeostasis
Claude Bernard, aunque menos enfocado en la microbiología, hizo contribuciones fundamentales a la fisiología y la medicina. Su concepto más influyente es el principio de la homeostasis, que él describió como el «milieu intérieur» (ambiente interno). Bernard sostuvo que la estabilidad del ambiente interno es crucial para la vida y que el cuerpo tiene mecanismos para mantener esta estabilidad frente a cambios externos. Este concepto es fundamental para la medicina moderna, ya que subraya la importancia de los sistemas reguladores del cuerpo, como se ve en el funcionamiento de los riñones, el corazón y el sistema endocrino.
Poco antes de morir, Louis Pasteur reconoció, en su famosa frase: “Claude Bernard tenía razón: el agente no es nada. El terreno lo es todo”.
Mi Aporte Final
La interacción entre las infecciones crónicas y las enfermedades cardiovasculares, particularmente la aterosclerosis, termina reflejando una complejidad en la que el equilibrio del ambiente interno del cuerpo juega un papel crucial en lo que se refiere a poder o no poder desarrollar ciertas afecciones.
Tenemos evidencia suficiente que es capaz de demostrar la importancia crucial del «milieu intérieur» en la asociación entre estos dos estados patológicos, de modo que nadie podría o debería sorprenderse de que las perturbaciones provocadas por infecciones crónicas pueden predisponer al desarrollo de enfermedades cardiovasculares.
Desde el punto de vista de Claude Bernard podemos considerar, más allá de la mera presencia de patógenos, como la respuesta del cuerpo a estos invasores y la capacidad de mantener la homeostasis es lo que determina realmente la progresión hacia la enfermedad. Así, la inflamación crónica resultante de infecciones podría ser vista no solo como una respuesta a los patógenos, sino como una señal de que el equilibrio interno está perturbado.
En este mundo donde la prevalencia de enfermedades crónicas sigue en aumento, la importancia de mantener un estilo de vida antiinflamatorio no puede ser subestimada. Este enfoque que llevo defendiendo desde hace años no solo busca reducir los síntomas de inflamación ya existentes, sino que también juega un papel crucial en la prevención de una serie de condiciones de salud que pueden ser exacerbadas por procesos inflamatorios crónicos, como las enfermedades cardiovasculares, la diabetes tipo 2, y ciertos tipos de cáncer.
La inflamación es una respuesta natural, COMPLETAMENTE NATURAL, del sistema inmunitario frente a infecciones y lesiones; pero cuando esta respuesta se vuelve crónica, puede desencadenar y perpetuar más enfermedades. Por lo tanto, lograr mantener un equilibrio en nuestra respuesta inmunitaria es esencial para nuestra salud general. Este equilibrio no se logra simplemente a través de intervenciones médicas, sino mediante la adopción de un estilo de vida que promueva la regulación natural y saludable de los procesos inflamatorios.
Alimentación Antiinflamatoria
Una dieta antiinflamatoria juega un papel central en el control de la inflamación. Alimentos ricos en ácidos grasos omega-3, como el salmón, las sardinas, las grasas y carnes de animales criados libres y en pasto, son conocidos por sus propiedades antiinflamatorias. Estos ácidos grasos ayudan a reducir la producción de moléculas inflamatorias y a mejorar la salud cardiovascular.
Ejercicio Regular
El ejercicio regular es otro componente crucial de un estilo de vida antiinflamatorio. La actividad física no solo va a ser capaz de ayudarte a mantener un peso saludable, lo cual reduce la carga sobre nuestro sistema inmunitario, sino que también promueve la liberación de hormonas que son beneficiosas para reducir la inflamación.
Manejo del Estrés
El estrés crónico es un conocido promotor de la inflamación. Técnicas de manejo del estrés como la meditación y la respiración profunda pueden ayudar a reducir los niveles de estrés y, por ende, disminuir la inflamación. La práctica regular de estas técnicas no solo podrá mejorar nuestra salud mental, sino que también tiene efectos positivos en nuestro sistema inmunitario.
Exposición a la Luz Solar
La exposición a la luz solar desempeña un papel crucial en la síntesis de vitamina D en la piel, esencial para la salud ósea y la regulación del sistema inmune. La luz solar también puede mejorar el estado de ánimo y aliviar los síntomas de depresión mediante la liberación de serotonina. Además, la exposición moderada al sol ayuda a regular los ritmos circadianos, mejorando así la calidad del sueño y los patrones de vigilia.
Sueño Adecuado
La falta de sueño ha sido vinculada con un aumento en los niveles de inflamación en el cuerpo. Un sueño adecuado y reparador es fundamental para permitir que el cuerpo se recupere y regule adecuadamente los procesos inflamatorios. Los adultos deben apuntar a obtener entre 7 y 9 horas de sueño por noche para optimizar la salud del sistema inmunitario.
Adoptar un estilo de vida antiinflamatorio es una estrategia integral que requiere atención constante y cambios conscientes en nuestras rutinas diarias. Estos ajustes no solo mejoran la calidad de vida, sino que también fortalecen nuestras defensas naturales, permitiendo que nuestro sistema inmunitario funcione de manera óptima sin caer en los extremos de una respuesta hiperactiva o insuficiente. La prevención de la inflamación a través de estas prácticas puede proporcionar un camino poderoso hacia una salud sostenible y una vida más larga y vigorosa.
Referencias
Naga Venkata K Pothineni, Swathi Subramany, Kevin Kuriakose, Lily F Shirazi, Francesco Romeo, Prediman K Shah, Jawahar L Mehta, Infections, atherosclerosis, and coronary heart disease, European Heart Journal, Volume 38, Issue 43, 14 November 2017, Pages 3195–3201,
Steinl, David & Kaufmann, Beat. (2015). Ultrasound Imaging for Risk Assessment in Atherosclerosis. International Journal of Molecular Sciences. 16. 9749-9769. 10.3390/ijms16059749.


